Jan V. Hirschmann, MD
Professor of Medicine, University of Washington School of Medicine, Staff Physician, Puget Sound VA Medical Center, Seattle, WA
Artigo original: Hirschmann JV. Fungal, bacterial, and viral infections of the skin. ACP Medicine. 2009;1-15.
[The original English language work has been published by DECKER INTELLECTUAL PROPERTIES INC. Hamilton, Ontario, Canada. Copyright © 2011 Decker Intellectual Properties Inc. All Rights Reserved.]
Agradecimentos: Figura 12 – Centers for Disease Control and Prevention Public Health Image Library.
Tradução: Soraya Imon de Oliveira
Revisão técnica: Dr. Lucas Santos Zambon
Apesar da ampla área de superfície e da exposição constante ao ambiente, a pele é bastante resistente à infecção. O fator protetor mais importante é o estrato córneo intacto, que consiste numa forte barreira lipoproteica formada na superfície cutânea pela epiderme subjacente. 1 Esta barreira impede a invasão de patógenos ambientais e seu característico ressecamento desestimula a colonização e o crescimento de muitos organismos que necessitam de umidade para sobreviver, como os bacilos gram-negativos. Em adição, o desprendimento constante das células epidérmicas impede que a maioria dos micróbios estabeleça residência permanente.
Por outro lado, alguns organismos se fixam às células da pele e nelas se reproduzem. A flora cutânea normal é constituída primariamente de bacilos e cocos gram-positivos aeróbicos, em densidades que variam de aproximadamente 102 organismos/cm2 na pele seca a 107 organismos/cm2 em áreas úmidas (p. ex., axila). 2 Esta população residente inibe a colonização das superfícies cutâneas por organismos danosos, ocupando os sítios de ligação existentes nas células epidérmicas, competindo por nutrientes, produzindo substâncias antimicrobianas e mantendo um pH cutâneo baixo (cerca de 5,5). Os organismos anaeróbios são escassos, exceto nas áreas ricas em glândulas sebáceas, como a face e o tórax. Nas partes mais profundas destes sítios, assim como nos folículos pilosos, os anaeróbios atingem concentrações da ordem 104 a 106 organismos/cm2.
As infecções cutâneas ocorrem diante da falha dos mecanismos de proteção da pele, em especial nas situações em que traumatismos, inflamação, maceração por umidade excessiva ou outros fatores causam ruptura do estrato córneo. Os organismos causadores de infecção podem ser oriundos da flora residente da própria vítima, seja da pele ou de membranas mucosas adjacentes, contudo muitos são originários de outras pessoas, animais ou do meio ambiente.
Infecções por dermatófitos
Os dermatófitos são mofos (um tipo de fungo) que podem infectar a pele, cabelo e unhas. Estes organismos incluem espécies de Trichophyton, Microsporum e Epidermophyton. São classificados em antropofílicos, zoofílicos ou geofílicos, dependendo de terem como fonte primária os seres humanos, animais ou o solo, respectivamente. As infecções por dermatófitos geofílicos são esporádicas, ocorrendo primariamente entre jardineiros e trabalhadores rurais.
Os dermatófitos zoofílicos (espécies de Trichophyton e Microsporum) podem ter uma gama de hospedeiros restritos (p. ex., Microsporum persicolor infecta apenas ratazanas) ou afligir muitos animais diferentes (p. ex., Trichophyton mentagrophytes pode infectar camundongos e outros roedores, cães, gatos e cavalos). As infecções humanas por espécies zoofílicas ocorrem após a exposição a numerosos animais, incluindo cães, gatos, cavalos, gado, porcos, roedores, aves, ouriços e ratazanas.
Os dermatófitos zoofílicos (espécies de Trichophyton e Microsporum) podem ter uma gama de hospedeiros restritos (p. ex., Microsporum persicolor infecta apenas ratazanas) ou afligir muitos animais diferentes (p. ex., Trichophyton mentagrophytes pode infectar camundongos e outros roedores, cães, gatos e cavalos). As infecções humanas por espécies zoofílicas ocorrem após a exposição a numerosos animais, incluindo cães, gatos, cavalos, gado, porcos, roedores, aves, ouriços e ratazanas.
Os dermatófitos antropofílicos são a causa mais comum de infecções cutâneas por fungos transmitidas por contato direto entre pessoas ou a partir da exposição a células cutâneas descamadas presentes no meio ambiente, onde os artrósporos conseguem sobreviver por vários meses. A inoculação direta dos esporos através de rachaduras na pele pode levar à germinação e subsequente invasão das camadas cutâneas superficiais.
As infecções por dermatófitos são mais frequentes em alguns grupos étnicos e indivíduos com imunidade celular comprometida. Muitas das infecções causadas por dermatófitos antropofílicos ocorrem com mais frequência entre indivíduos de um determinado sexo ou faixa etária. A infecção do couro cabeludo, por exemplo, é primariamente uma doença da infância. O envolvimento dos pés e virilha é mais comum em adolescentes e adultos jovens, sobretudo entre os homens, mas é infrequente em crianças. A infecção da unha é mais frequente em indivíduos de idade avançada de ambos os sexos. As causas destas diferenças são desconhecidas.
Os dermatófitos antropofílicos também seguem padrões de distribuição geográfica exclusivos. Nos Estados Unidos, o causador de infecção no couro cabeludo mais comum é Trichophyton tonsurans.
No Sudeste da Ásia e Oriente Médio, esta infecção é causada principalmente por Trichophyton violaceum. É possível que estas diferenças estejam relacionadas a fatores climáticos ou raciais.
No Sudeste da Ásia e Oriente Médio, esta infecção é causada principalmente por Trichophyton violaceum. É possível que estas diferenças estejam relacionadas a fatores climáticos ou raciais.
As várias formas de dermatofitose, também denominadas tineas, são nomeadas de acordo com o sítio de envolvimento. Estas infecções incluem a tinea captis (couro cabeludo), tinea corporis (corporal), tinea barbae (área da barba masculina), tinea faciei (rosto), tinea cruris (virilha), tinea pedis (pés), tinea unguium (unhas) e tinea manuum (mãos). A lesão cutânea característica consiste numa placa escamosa anular [Figura 1], embora o aspecto clínico varie não só conforme o sítio de envolvimento como também de acordo com a condição imunológica do hospedeiro e o tipo de organismo infeccioso.
Em geral, as espécies antropofílicas deflagram pouca inflamação e causam infecções crônicas. As espécies zoofílicas e geofílicas, por outro lado, costumam provocar uma inflamação intensa, que às vezes resulta na erradicação dos organismos e é resolvida sem tratamento.
Em geral, as espécies antropofílicas deflagram pouca inflamação e causam infecções crônicas. As espécies zoofílicas e geofílicas, por outro lado, costumam provocar uma inflamação intensa, que às vezes resulta na erradicação dos organismos e é resolvida sem tratamento.
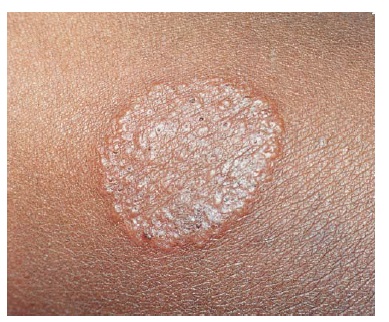
Figura 1. Lesão anular clássica da tinea corporis, mostrando uma margem vesicular ou saliente com uma região central clara.
Manifestações clínicas
Tinea Captis (couro cabeludo)
A tinea captis ocorre primariamente em crianças, mas pode se desenvolver em adultos – sobretudo em indivíduos idosos, malcuidados e enfraquecidos. 3 A transmissão pode ocorrer entre seres humanos, através do compartilhamento de pentes, escovas ou acessórios para a cabeça. Somente as espécies de Microsporum e Trichophyton causam tinea captis. A infecção começa com a invasão do estrato córneo da pele do couro cabeludo. Os cabelos então são infectados, segundo 1 dentre 3 padrões microscópicos: ectotrix, endotrix ou favo. No ectotrix, os esporos são encontrados do lado externo da haste do cabelo e destroem a cutícula. No endotrix, os esporos ficam junto ao cabelo e não afetam a cutícula. E no favo, há formação de amplas hifas e espaços de ar junto ao cabelo, porém os esporos estão ausentes.
Em todos estes 3 tipos, a formação de cicatriz, perda de cabelo e inflamação de graus variados.
Em todos estes 3 tipos, a formação de cicatriz, perda de cabelo e inflamação de graus variados.
Trichophyton tonsurans, principal causador da tinea captis em adultos, caracteristicamente produz uma infecção não inflamatória com áreas de descamação e alopecia que podem ser tanto bem demarcadas como difusas e irregulares. Como os cabelos inchados podem se quebrar há alguns milímetros da epiderme na infecção do tipo endotrix, o couro cabeludo às vezes parece ter pequenas marcas em forma de pontos negros acentuados. Assim como em todas as manifestações produzidas por espécies de Trichophyton, estas lesões no couro cabeludo não emitem fluorescência sob luz de Wood.
A inflamação mais severa, usualmente produzida por uma espécie zoofílica, resulta em um quérion – uma massa dolorosa de aspecto encharcado, onde pode haver formação de tratos sinusais e os folículos podem secretar pus [Figura 2]. É comum haver formação de crosta e embaçamento dos pelos adjacentes. Pode haver ampliação dos linfonodos cervicais.
A inflamação mais severa, usualmente produzida por uma espécie zoofílica, resulta em um quérion – uma massa dolorosa de aspecto encharcado, onde pode haver formação de tratos sinusais e os folículos podem secretar pus [Figura 2]. É comum haver formação de crosta e embaçamento dos pelos adjacentes. Pode haver ampliação dos linfonodos cervicais.
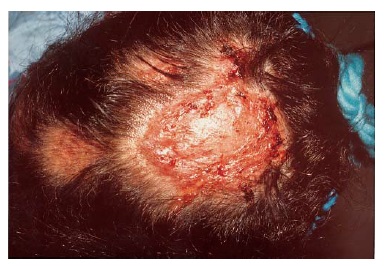
Figura 2. Um quérion típico, que se manifesta como infecção zoofílica do couro cabeludo por Microsporum canis (tinea captis).
Tinea Corporis (corpo)
A tinea corporis tipicamente se manifesta como uma lesão isolada ou como múltiplas lesões circulares que apresentam escamação, margens bem delineadas e uma borda saliente e eritematosa. Com frequência, há desenvolvimento de uma área central clara. A quantidade de inflamação varia e, quando intensa, pode haver formação de pústulas, vesículas e até bolhas. Às vezes o envolvimento dos folículos pilosos no meio de uma placa de escamação eritematosa leva ao desenvolvimento de nódulos perifoliculares, numa condição conhecida como granuloma de Majocchi. Esta condição usualmente ocorre nas pernas dos pacientes infectados por Trichophyton rubrum e pode ser precipitada pela terapia tópica à base de corticosteroides. Em hospedeiros imunocomprometidos, pode haver desenvolvimento de abscessos subcutâneos.
Tinea Barbae (barba)
A tinea barbae ocorre em homens adultos. Envolve a pele e os pelos grossos da barba e da região do bigode. Sua causa usual são as espécies zoofílicas, primariamente Trichophyton verrucosum e Trichophyton mentagrophytes, que comumente infectam bovinos e equinos. As vítimas em geral são trabalhadores de fazenda. A infecção usualmente causa eritema, escamação e pústulas foliculares. Muitos pelos tornam-se frouxos e facilmente removíveis com auxílio de pinça.
Tinea Faciei (face)
A tinea faciei ocorre como infecção da face em mulheres e crianças. Nos homens, ocorre como infecção da área localizada fora das regiões de bigode e barba. Suas causas usuais são Trichophyton rubrum e Trichophyton mentagrophytes. Estes organismos atingem a face via inoculação direta ou por meio da disseminação a partir de outro sítio de infecção corporal. Os pacientes costumam se queixar de prurido e ardência, sendo que os sintomas podem piorar após a exposição à luz solar. As lesões podem ser placas eritematosas anulares e escamosas, mas frequentemente consistem em áreas avermelhadas indistintas apresentando pouca ou nenhuma escamação.
Tinea Cruris (virilha)
A tinea cruris, que consiste na infecção da virilha, é bem mais comum em homens do que nas mulheres e frequentemente está associada à infecção dos pés. Suas causas mais comuns são Trichophyton rubrum, Trichophyton mentagrophytes e Epidermophyton floccosum. As lesões em geral são áreas avermelhadas, escamosas e agudamente demarcadas, com bordas salientes e eritematosas. A infecção, que afeta a porção média das região superior das coxas, poupando consistentemente o escroto, pode se estender para as nádegas, abdômen e região lombar. Pode haver formação de vesículas, nódulos e pústulas, além de maceração.
Tinea Pedis (pés)
A tinea pedis é mais frequentemente causada por Trichophyton rubrum, Epidermophyton floccosum e Trichophyton mentagrophytes. Sua forma mais comum envolve a fissura, escamação e maceração dos espaços interdigitais, sobretudo entre o 4º e 5º dedos do pé. Estes achados também são encontrados no eritrasma (veja adiante). Um segundo tipo envolve a escamação, hiperceratose e eritema das solas dos pés, calcanhares e laterais dos pés. Neste tipo de tinea pedis, as lesões seguem um padrão de distribuição conhecido como mocassim, afetando as solas, dedos e laterais dos pés [Figura 3a]. A pele plantar pode se tornar bastante espessa e escamosa. Uma terceira forma de tinea pedis segue um padrão inflamatório, caracterizado pela formação de vesículas, pústulas ou até bolhas, geralmente nas solas dos pés [Figura 3b].
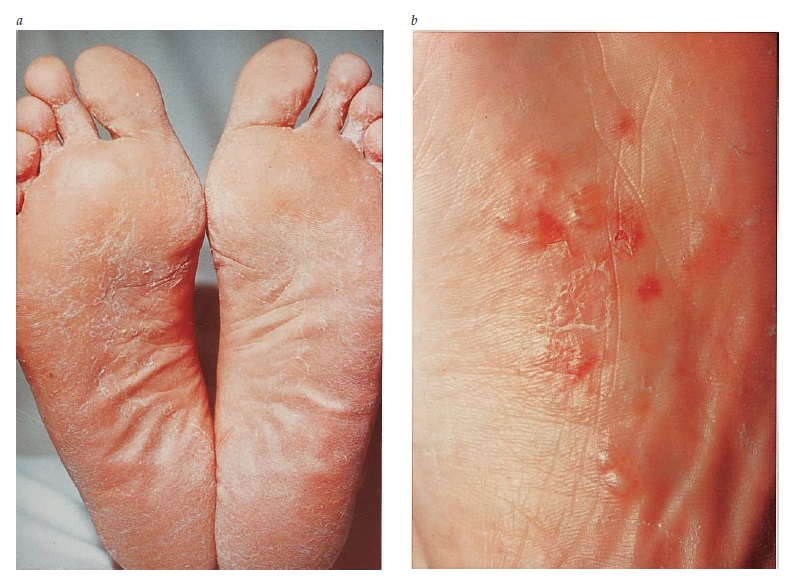
Figura 3. (a) A descamação associada à tinea pedis surge entre e embaixo dos dedos do pé, e também na superfície plantar. (b) A tinea pedis também pode se manifestar como vesículas.
Uma complicação importante da tinea pedis é a celulite estreptocócica na região inferior da perna. Os estreptococos não costumam sobreviver na pele normal, mas a existência de uma doença fúngica parece permitir que estreptococos de vários grupos (incluindo A, B, C e G) colonizem as pregas interdigitais dos pés. 5 A partir desta localização, as bactérias podem invadir a pele danificada pela tinea pedis ou migrar para as partes mais superiores da perna e penetrar a pele através de um defeito qualquer.
Tinea Unguium (unhas)
A tinea unguium (ou onicomicose) é bastante comum na população em geral: um extensivo estudo conduzido na Europa registrou uma prevalência de quase 30%, com os idosos apresentando um risco maior de infecção, em comparação aos indivíduos mais jovens. 5 Em sua forma mais comum, os organismos invadem a unha a partir das bordas distais ou laterais, e a disseminação se dá ao nível proximal.
As unhas tornam-se espessas, opacas e adquirem uma tonalidade amarela a marrom. Podem rachar ou esmigalhar. A hiperceratose subungueal frequentemente eleva a placa ungueal em relação ao leito subjacente (uma condição conhecida como onicolise)[Figura 4]. As hemorragias por fragmentação são comuns.
Na onicomicose branca superficial, placas esbranquiçadas calcárias surgem na superfície da unha, que se torna mole e friável. Na onicomicose subungueal proximal, a forma mais comumente observada em pacientes imunocomprometidos, incluindo aqueles infectados pelo vírus da imunodeficiência humana (HIV), o fungo envolve a região da unha situada embaixo da cutícula e causa infecção o leito ungueal proximal.
As unhas tornam-se espessas, opacas e adquirem uma tonalidade amarela a marrom. Podem rachar ou esmigalhar. A hiperceratose subungueal frequentemente eleva a placa ungueal em relação ao leito subjacente (uma condição conhecida como onicolise)[Figura 4]. As hemorragias por fragmentação são comuns.
Na onicomicose branca superficial, placas esbranquiçadas calcárias surgem na superfície da unha, que se torna mole e friável. Na onicomicose subungueal proximal, a forma mais comumente observada em pacientes imunocomprometidos, incluindo aqueles infectados pelo vírus da imunodeficiência humana (HIV), o fungo envolve a região da unha situada embaixo da cutícula e causa infecção o leito ungueal proximal.
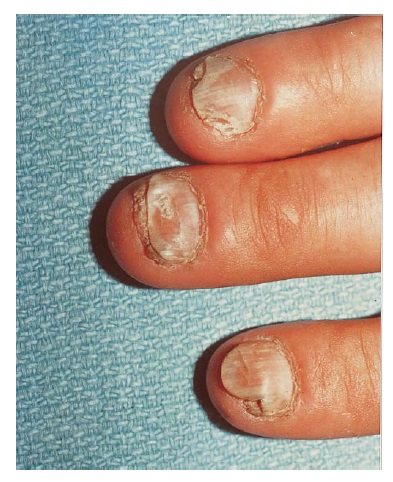
Figura 4. As unhas usualmente estão espessadas, rachadas e quebradiças na tinea unguium. Como se observa, pode haver debris subungueais.
Tinea Manuum (mãos)
A tinea manuum é uma infecção das mãos. A maioria dos casos é acompanhada do envolvimento dos pés. De modo inexplicável, em geral apenas uma das mãos (não necessariamente a dominante) é afetada (condição conhecida como doença de 2 pés e 1 mão). O achado mais comum é a escamação ou hiperceratose das palmas e dedos da mão. Ocasionalmente, há formação de vesículas, pápulas ou nódulos foliculares na superfície dorsal das mãos.
Diagnóstico
Os clínicos devem suspeitar de infecção por dermatófitos diante de pacientes que apresentem erupções eritematosas escamosas, bem como em casos de pacientes com unhas que apresentem características de tinea unguium (veja anteriormente). O diagnóstico pode ser confirmado por microscopia ou cultura de amostras corretamente coletadas. O método ideal de obtenção de amostras a partir da pele consiste na raspagem das lesões escamosas. As melhores amostras oriundas das unhas são fragmentos de debris subungueais. 6
Na preparação para o exame microscópico, a amostra é primeiramente colocada em uma lâmina de vidro e tratada com hidróxido de potássio (KOH), que digere a queratina contida na pele, unhas e cabelo. Em seguida, a amostra é aquecida para acelerar o processo. Nas mãos de profissionais experientes, esta abordagem possui alta sensibilidade e especificidade para a detecção de dermatófitos. Uma técnica alternativa consiste no uso de calcoflúor, que se liga à celulose e à quitina presentes na parede das células fúngicas e emite fluorescência ao ser exposta à radiação ultravioleta. A sensibilidade desta técnica é um pouco maior do que a sensibilidade das preparações de KOH, mas requer um microscópio de fluorescência.
O meio de cultura básico para isolamento de dermatófitos é o ágar contendo meio Sabouraud, que frequentemente é combinado a antibióticos (para eliminar as bactérias) e ciclo-heximida (para inibir fungos saprofíticos). O crescimento usualmente se torna evidente em 3-14 dias. O meio de cultura empregado no teste de dermatófitos pode ser usado no consultório, além de ser acurado e econômico. Quando as preparações microscópicas e culturas resultam negativas ou como alternativa às culturas, uma biópsia pode ser útil para identificar o organismo infectante, em geral por meio de colorações teciduais especiais, como a coloração com ácido periódico de Schiff ou as preparações de metenamina-prata de Gomori.
Infecções por levedura
As leveduras são fungos unicelulares que se reproduzem por brotamento. Podem formar projeções filamentosas que, diferente das hifas dos bolores, não contêm células isoladas. Do mesmo modo, são chamadas pseudo-hifas. As espécies de Candida não fazem parte da flora cutânea normal, mas costumam residir na orofaringe, vagina e cólon. A partir destas localizações, podem causar infecções na pele adjacente traumatizada. Alternativamente, com a redução de outras floras ou diante do comprometimento dos mecanismos de defesa do hospedeiro, estas leveduras podem proliferar e atingir números amplos, produzindo lesões nas superfícies mucosas da boca e vagina.
Malassezia furfur (também chamada de Pityrosporum orbiculare ou Pityrosporum ovale) é uma levedura que precisa de lipídios para crescer. Normalmente, coloniza a pele de indivíduos adultos, sobretudo no couro cabeludo e parte superior do tronco, onde a presença de sebo é maior. Por motivos desconhecidos, estes organismos (que são ordinariamente comensais) podem se tornar patogênicos e causar tinea versicolor (também conhecida como pitiríase versicolor) ou foliculite. Evidências convincentes sugerem que estes organismos também causam dermatite seborreica e caspa.
Candidíase
Manifestações clínicas
Candidíase oral. Uma forma de candidíase oral, o sapinho, surge como placas de cor branca a cinza (pseudomembranas) sobre a língua, palato mole, gengiva, orofaringe e mucosa bucal. A remoção de material oriundo da superfície mucosa revela a existência de uma base eritematosa subjacente.
Os fatores predisponentes encontrados em indivíduos adultos são o diabetes melito, uso sistêmico ou local de corticosteroides, administração de antibióticos de amplo espectro, radio ou quimioterapia, e imunidade celular comprometida (sobretudo em consequência de infecção por HIV). A candidíase atrófica aguda em especial segue-se à terapia antibiótica e produz lesões dolorosas, avermelhadas e expostas nas membranas mucosas. A língua pode apresentar áreas eritematosas com papilas filiformes atróficas.
Na candidíase atrófica crônica, a contaminação de dentaduras por Candida resulta em lesões dolorosas, avermelhadas e por vezes edematosas, com epitélio reluzente e atrófico e bordas bem demarcadas no ponto de contato entre a dentadura e as membranas mucosas. A falta de higiene dental e o uso prolongado de dentadura são fatores predisponentes comuns.
Alguns pacientes que apresentam tais fatores desenvolvem queilite angular (perleche), caracterizada por eritema e fissura dos cantos da boca. Outras condições que contribuem para a queilite angular são a maceração por excesso de salivação ou lambição; dentaduras mal ajustadas; e uma dobra maior resultante da diminuição da altura da crista alveolar. Candida está presente na maioria (mas não em todos) dos pacientes com este distúrbio.
Os fatores predisponentes encontrados em indivíduos adultos são o diabetes melito, uso sistêmico ou local de corticosteroides, administração de antibióticos de amplo espectro, radio ou quimioterapia, e imunidade celular comprometida (sobretudo em consequência de infecção por HIV). A candidíase atrófica aguda em especial segue-se à terapia antibiótica e produz lesões dolorosas, avermelhadas e expostas nas membranas mucosas. A língua pode apresentar áreas eritematosas com papilas filiformes atróficas.
Na candidíase atrófica crônica, a contaminação de dentaduras por Candida resulta em lesões dolorosas, avermelhadas e por vezes edematosas, com epitélio reluzente e atrófico e bordas bem demarcadas no ponto de contato entre a dentadura e as membranas mucosas. A falta de higiene dental e o uso prolongado de dentadura são fatores predisponentes comuns.
Alguns pacientes que apresentam tais fatores desenvolvem queilite angular (perleche), caracterizada por eritema e fissura dos cantos da boca. Outras condições que contribuem para a queilite angular são a maceração por excesso de salivação ou lambição; dentaduras mal ajustadas; e uma dobra maior resultante da diminuição da altura da crista alveolar. Candida está presente na maioria (mas não em todos) dos pacientes com este distúrbio.
A candidíase hiperplásica crônica (leucoplaquia da candidíase) consiste na formação de placas irregulares, esbranquiçadas e persistentes sobre a língua ou membranas mucosas, que são difíceis de remover. Esta forma de candidíase ocorre especialmente em fumantes do sexo masculino. Dor, ardência e aspereza nas áreas afetadas constituem os sintomas usuais. A candidíase da língua também pode assumir a forma de glossite romboide mediana, que consiste numa área em formato de diamante constituída de papilas atróficas na porção central da superfície lingual.
Intertrigo da candidíase. A infecção por Candida pode ocorrer em qualquer dobra cutânea, causando dor e prurido. Os pacientes obesos são especialmente vulneráveis. As áreas comumente afetadas incluem a virilha, regiões inframamárias e dobras do pano abdominal, porém até mesmo os espaços interdigitais podem ser envolvidos. As lesões consistem em placas de eritema brilhante acompanhadas de maceração, com uma borda irregular e recortada, além das quais é comum observar pápulas e pústulas (lesões satélite) [Figura 5].
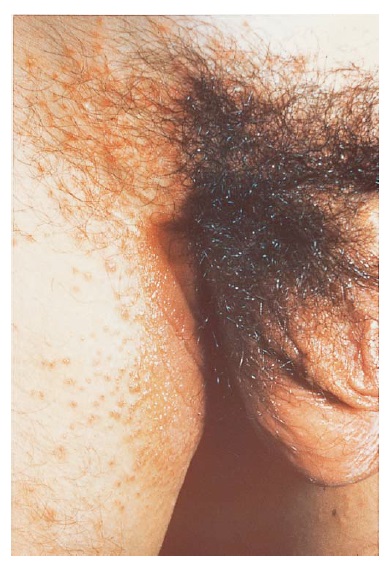
Figura 5. Lesões satélite proeminentes de vesículas discretas observadas em um paciente com candidíase.
Balanite e vulvovaginite da candidíase. A maioria das mulheres com vulvovaginite da candidíase não apresenta doença subjacente. Contudo, esta condição pode ser acompanhada de diabetes melito e infecção por HIV, e também pode ocorrer como complicação da terapia com certos antibióticos.
A vulvovaginite da candidíase leva ao aparecimento de placas esbranquiçadas sobre uma mucosa vaginal avermelhada e inchada; secreção vaginal de aspecto cremoso; e eritema (às vezes com pústulas) na pele vulvar. A dor e a ardência são sintoma comuns.
Os parceiros do sexo masculino de mulheres com vulvovaginite da candidíase podem desenvolver uma balanite caracterizada por eritema, pústulas e erosões na glande do pênis.
A balanite pode ocorrer de modo espontâneo, mas por vezes indica a presença de diabetes melito.
A vulvovaginite da candidíase leva ao aparecimento de placas esbranquiçadas sobre uma mucosa vaginal avermelhada e inchada; secreção vaginal de aspecto cremoso; e eritema (às vezes com pústulas) na pele vulvar. A dor e a ardência são sintoma comuns.
Os parceiros do sexo masculino de mulheres com vulvovaginite da candidíase podem desenvolver uma balanite caracterizada por eritema, pústulas e erosões na glande do pênis.
A balanite pode ocorrer de modo espontâneo, mas por vezes indica a presença de diabetes melito.
Infecção da unha e paroniquia da candidíase.
A maceração do tecido que circunda a unha, tipicamente resultante do excesso de umidade, pode causar paroniquia. A paroniquia é caracterizada por eritema, inchaço e dor na prega da unha, acompanhados de perda de cutícula [Figura 6].
Os organismos de Candida frequentemente colonizam a área, mas são provavelmente patogênicos somente quando há formação de pus. Com a colonização crônica, pode haver envolvimento da unha, com consequente produção de uma tonalidade amarelada e separação da placa da unha em relação ao leito ungueal (onicolise).
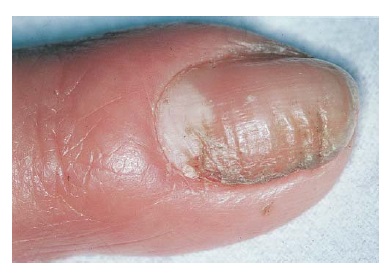
Figura 6. Em uma paroniquia de candidíase, observada no polegar deste paciente, a prega da unha se tornou avermelhada, inchada e dolorosa. A distrofia da unha também é observada.
Diagnóstico
Os raspados das lesões de membranas mucosas ou cutâneas podem ser misturados a uma solução de KOH e examinados ao microscópio quanto à presença de brotamentos de leveduras com pseudo-hifas. As colorações de Gram de uma mesma amostra, todavia, são mais facilmente avaliáveis, pois revelam a presença de organismos gram-positivos, ovais e bem amplos, que podem apresentar brotamentos ou formação de pseudo-hifas. Estas leveduras são bem maiores do que as bactérias e podem ser mais facilmente observadas em amostras coradas pelo método de Gram, do que em preparações de KOH. A cultura de amostras pode ser útil, se a microscopia resultar normal ou ambígua. Estes organismos crescem rápido tanto em meios para fungos como nos meios para bactérias convencionais.
Infecções por Malassezia
Manifestações clínicas
Tinea versicolor. Usualmente assintomática, a tinea versicolor pode causar prurido ou irritação cutânea. As lesões consistem em pequenas manchas discretas, que tendem a ser mais escuras do que a pele circundante em pacientes de pele clara e hipopigmentadas em pacientes de pele escura. Estas lesões costumam coalescer, formando placas amplas de diversas cores (versicolor), que variam do branco ao marrom claro [Figura 7]. A raspagem das lesões produz escamas finas. Esta infecção mais comumente envolve parte superior do tronco, porém os braços, axilas, abdome e virilha também podem ser afetados. A maioria das lesões exibe fluorescência amarelada sob luz de Wood.
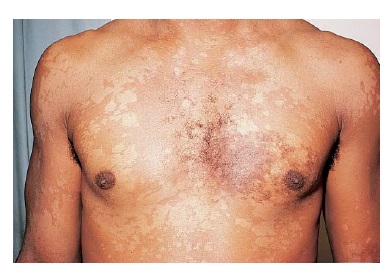
Figura 7. Uma tinea versicolor aprece no tórax deste paciente, sob a forma de manchas ovais, hipopigmentadas e finamente descamadas.
Foliculite por Malassezia (foliculite por Pityrosporum). Na foliculite, a inflamação dos folículos pilosos causa o aparecimento de pápulas avermelhadas e pústulas que circundam os fios de cabelo individualmente. Várias espécies de Malassezia causam foliculite. As lesões predominam no tronco, mas ocasionalmente também podem aparecer nos braços. A ausência de comedões permite distinguir entre a lesão da foliculite e a lesão acneica. Pode haver prurido e formigamento.
Diagnóstico
Em pacientes com tinea versicolor, a preparações de KOH de raspados de lesão mostram a presença de pseudo-hifas e leveduras, cujo aspecto pode ser semelhante ao de espaguete com almôndegas. Esta técnica é suficiente para estabelecer o diagnóstico. A forma de levedura prevalece na foliculite e é facilmente observada em amostras purulentas de pústula coradas pelo método de Gram, onde aparece como um organismo gram-positivo oval e grande, que é significativamente maior do que uma bactéria. As biópsias destas lesões mostram a presença de leveduras ao redor e dentro dos folículos pilosos, acompanhadas de inflamação neutrofílica. Os organismos são mais nitidamente observados em amostras coradas com ácido periódico de Schiff ou metenamina-prata de Gomori. Como estas leveduras fazem parte da flora normal da pele, seu crescimento em culturas de raspados de superfície cutânea não têm utilidade diagnóstica. A cultura do organismo a partir do pus da foliculite, porém, é definitiva. Contudo, este tipo de cultura requer meio especial, como ágar Sabouraud com azeite de oliva, para fornecimento do conteúdo lipídico necessário à nutrição dos organismos. O crescimento tipicamente ocorre em 3-5 dias.
Infecções bacterianas
Infecções cutâneas causadas por estreptococos, estafilococos ou ambos
Impetigo
Inicialmente, uma infecção cutânea vesicular, o impetigo não bolhoso evolui rápido para pústulas que então se rompem e liberam uma secreção que, ao secar, forma crostas cor-de-mel sobre uma base eritematosa [Figura 8].11
As lesões com frequência são pruriginosas. O impetigo não bolhoso ocorrem de modo característico na pele previamente danificada por traumatismos, como abrasões ou cortes. As áreas expostas são mais comumente envolvidas, de forma típica os membros ou as áreas localizadas ao redor da boca e do nariz. O impetigo não bolhoso é uma doença contagiosa, usualmente de crianças pequenas. É mais frequente em regiões de clima quente e úmido, do que nas áreas temperadas, e sua ocorrência costuma estar associada a condições de falta de higiene e ambientes lotados.
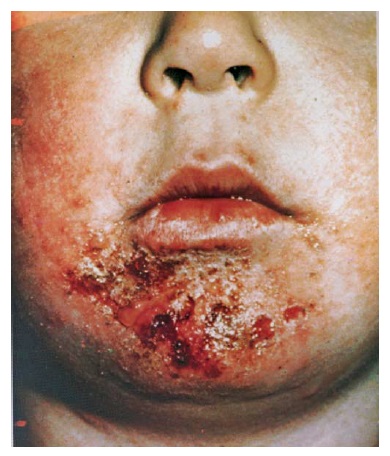
Figura 8. As vesículas-pústulas ou bolhas do impetigo se rompem rapidamente e deixam uma base eritematosa coberta por uma camada delgada de exsudato seropurulento. O exsudato seca e forma camadas de crostas cor-de-mel.
A causa mais comum de impetigo não bolhoso é o Staphylococcus aureus, mas às vezes Streptococcus pyogenes (estreptococos do grupo A) também estão presentes. Ocasionalmente, o S. Pyogenes é o único organismo a crescer em cultura. Algumas cepas de S. Aureus elaboram toxinas que causam a ruptura da epiderme e o desenvolvimento de bolhas de paredes delgadas. Neste distúrbio, conhecido como impetigo bolhoso, há formação de pústulas vesiculares superficiais, frágeis e flácidas. Estas pústulas vesiculares então se rompem e liberam um exsudato que, ao secar, origina uma crosta delgada, de cor marrom e aspecto envernizado. Em alguns casos, as pústulas vesiculares não se tornam evidentes e as erosões eritematosas (frequentemente circundadas por um colar de resquícios de parede de bolhas) constituem o único distúrbio evidente. Os aglomerados de cocos gram-positivos em geral são evidenciados pela coloração de Gram de amostras do líquido ou pus oriundo das bolhas ou da superfície das erosões. O crescimento de S. Aureus em culturas produzidas com estas amostras estabelece o diagnóstico de impetigo bolhoso.
O crescimento de S. Aureus, S. Pyogenes ou ambos a partir de lesões cutâneas decorrentes de impetigo não bolhoso confirma o diagnóstico de impetigo não bolhoso. Entretanto, as culturas são desnecessárias nos casos característicos. Para o tratamento de lesões esparsas e não bolhosas, a aplicação tópica de uma pomada de mupirocina (3 vezes/dia, por 7 dias) é tão efetiva quanto o uso de agentes antimicrobianos orais. Alternativamente, um agente antimicrobiano efetivo de uso tópico é a pomada de retapamulina, aplicada 2 vezes/dia por 5 dias. Os antibióticos sistêmicos ativos contra S. Aureus e S. Pyogenes, como a cefalexina ou a dicloxacilina, são preferíveis à terapia tópica para pacientes com numerosas lesões, além de serem o tratamento de escolha para o impetigo bolhoso. Até agora, Staphylococcus aureus resistente à meticilina (SARM) raramente é isolado em casos de impetigo, sendo que os agentes ativos contra este organismo ainda não se fazem necessários para o sucesso do tratamento empírico. Devido à natureza superficial destas infecções, as lesões são curadas sem formação de cicatriz.
Ectima
O ectima é uma infecção mais profunda do que o impetigo. Assim como no impetigo não bolhoso, S. Aureus, S. Pyogenes ou ambos podem ser a causa da condição. O ectima ocorre com frequência em pacientes que vivem sob condições de higiene precária, desnutrição ou que sofreram traumatismo prévio. As lesões, que costumam ser múltiplas e mais comuns nos membros inferiores, surgem como vesículas. Estas vesículas se rompem e criam lesões circulares e eritematosas, com crostas aderentes. Por baixo destas crostas, que podem se formar espontaneamente, existem úlceras que deixam cicatriz ao serem resolvidas. A cultura de material oriundo da base das úlceras resulta no crescimento dos organismos causadores da condição. O tratamento deve consistir na administração oral de um agente antiestafilocócico, como dicloxacilina ou cefalexina.
Infecções cutâneas causadas por estreptococos
Celulite e erisipela
A celulite e a erisipela são infecções cutâneas agudas e disseminadas, causadas primariamente por vários estreptococos, incluindo aqueles dos grupos A, B, C, F e G. O termo erisipela possui vários significados. Um deles descreve uma infecção em que há envolvimento da derme superficial, sobretudo dos linfáticos dérmicos, enquanto a celulite afeta a derme mais profunda e o tecido adiposo subcutâneo. De acordo com esta definição, as erisipelas (mas não a celulite) exibem uma borda elevada e precisamente demarcada. As diferenças em termos de manifestação clínica entre ambas, porém, geralmente são irrelevantes e muitas vezes confusas. Os sítios mais comuns destas infecções são a face e os membros inferiores.
Os organismos causais podem penetrar a pele em áreas evidentes, como feridas produzidas por traumatismo e úlceras na perna, ou via inflamação cutânea (p. Ex., eczema). Entretanto, na maioria dos casos, não há nenhum ponto de entrada evidente. O edema produzido por causas diversas, entre as quais a insuficiência venosa, hipoalbuminemia e insuficiência linfática, constitui o fator predisponente. A infecção comumente ocorre na pele exposta a danos permanentes, como queimaduras, traumatismos, radioterapia ou cirurgia. A celulite, por exemplo, pode ocorrer em um sítio de remoção de veia safena para cirurgia cardíaca ou vascular, passados meses a anos da realização do procedimento.12
Um fator predisponente importante em pacientes com erisipela ou celulite na perna é o impetigo no dedo do pé (fissura e maceração entre os dedos do pé, usualmente representando uma infecção por dermatófitos ou eritrasma, discutidos adiante). Os estreptococos que colonizam estas áreas podem invadir a pele localmente ou migrar para regiões mais proximais da perna e penetrar a pele anômala. A idade avançada e a obesidade também constituem fatores predisponentes.13
Os organismos causais podem penetrar a pele em áreas evidentes, como feridas produzidas por traumatismo e úlceras na perna, ou via inflamação cutânea (p. Ex., eczema). Entretanto, na maioria dos casos, não há nenhum ponto de entrada evidente. O edema produzido por causas diversas, entre as quais a insuficiência venosa, hipoalbuminemia e insuficiência linfática, constitui o fator predisponente. A infecção comumente ocorre na pele exposta a danos permanentes, como queimaduras, traumatismos, radioterapia ou cirurgia. A celulite, por exemplo, pode ocorrer em um sítio de remoção de veia safena para cirurgia cardíaca ou vascular, passados meses a anos da realização do procedimento.12
Um fator predisponente importante em pacientes com erisipela ou celulite na perna é o impetigo no dedo do pé (fissura e maceração entre os dedos do pé, usualmente representando uma infecção por dermatófitos ou eritrasma, discutidos adiante). Os estreptococos que colonizam estas áreas podem invadir a pele localmente ou migrar para regiões mais proximais da perna e penetrar a pele anômala. A idade avançada e a obesidade também constituem fatores predisponentes.13
Diagnóstico. Os achados cutâneos incluem um eritema em rápida expansão e o inchaço da pele [Figura 9], por vezes acompanhado de estrias avermelhadas proximais, representativas de linfangite, além de linfonodos regionais ampliados. Pode haver vesículas, bolhas, petéquias e equimoses.
A superfície cutânea pode exibir um aspecto semelhante ao de casca de laranja (peau d’orange), pois os folículos pilosos permanecem fracamente em contato com as estruturas mais profundas, mantendo suas aberturas abaixo do edema superficial circundante e criando as características ondulações cutâneas. Na face, a localização típica é sobre uma ou ambas as bochechas, muitas vezes com um padrão de eritema e inchaço em forma de “borboleta”. A extensão para as pálpebras, orelhas ou pescoço é comum. Os sintomas sistêmicos, como febre, cefaleia e confusão, podem acompanhar estas infecções. Às vezes, estes sintomas precedem em várias horas a detecção de quaisquer achados cutâneos ao exame. Há pacientes que não apresentam manifestações sistêmicas, embora exibam anormalidades cutâneas graves.
A superfície cutânea pode exibir um aspecto semelhante ao de casca de laranja (peau d’orange), pois os folículos pilosos permanecem fracamente em contato com as estruturas mais profundas, mantendo suas aberturas abaixo do edema superficial circundante e criando as características ondulações cutâneas. Na face, a localização típica é sobre uma ou ambas as bochechas, muitas vezes com um padrão de eritema e inchaço em forma de “borboleta”. A extensão para as pálpebras, orelhas ou pescoço é comum. Os sintomas sistêmicos, como febre, cefaleia e confusão, podem acompanhar estas infecções. Às vezes, estes sintomas precedem em várias horas a detecção de quaisquer achados cutâneos ao exame. Há pacientes que não apresentam manifestações sistêmicas, embora exibam anormalidades cutâneas graves.
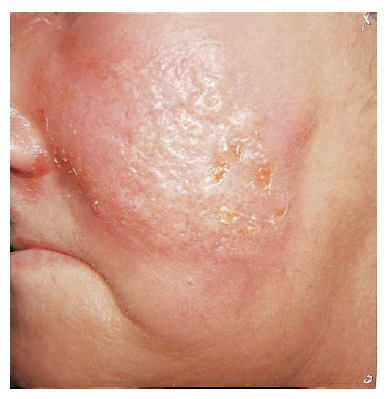
Figura 9. Eritema, edema e demarcação precisa da lesão a partir da pele circundante normal caracterizam a erisipela facial.
O diagnóstico é amplamente clínico. Em um caso típico, as culturas são desnecessárias e usualmente não há benefício em se realizar a coleta. A aspiração da lesão com agulha fornece um isolado em cerca de 5-20% das amostras. As hemoculturas obtidas de pacientes febris resultam positivas em menos de 5% dos casos e, por causa deste rendimento baixo, tornam-se desnecessárias nos casos típicos de celulite.14
As biópsias por punção da pele fornecem culturas positivas em cerca de 20% dos casos.15 Estes resultados, aliados aos resultados dos testes sorológicos de anticorpos para estreptococos16 e ensaios de imunofluorescência de biópsias de pele,17 indicam que os estreptococos causam a vasta maioria (provavelmente cerca de 90%) dos casos de celulite e erisipela na ausência de traumatismo penetrante, abscessos ou outras condições mencionadas adiante. A celulite produzida por S. Aureus geralmente ocorre na presença de um abscesso ou lesão penetrante, inclusive as injeções de drogas ilícitas. As circunstâncias adicionais em que outros organismos, além dos estreptococos, tendem a ser responsáveis pelos casos de celulite incluem a imunodeficiência, traumatismo com penetração, lesões por imersão em água doce ou salgada, granulocitopenia e mordidas ou arranhaduras produzidas por animais. As culturas são apropriadas em todas estas situações.
As biópsias por punção da pele fornecem culturas positivas em cerca de 20% dos casos.15 Estes resultados, aliados aos resultados dos testes sorológicos de anticorpos para estreptococos16 e ensaios de imunofluorescência de biópsias de pele,17 indicam que os estreptococos causam a vasta maioria (provavelmente cerca de 90%) dos casos de celulite e erisipela na ausência de traumatismo penetrante, abscessos ou outras condições mencionadas adiante. A celulite produzida por S. Aureus geralmente ocorre na presença de um abscesso ou lesão penetrante, inclusive as injeções de drogas ilícitas. As circunstâncias adicionais em que outros organismos, além dos estreptococos, tendem a ser responsáveis pelos casos de celulite incluem a imunodeficiência, traumatismo com penetração, lesões por imersão em água doce ou salgada, granulocitopenia e mordidas ou arranhaduras produzidas por animais. As culturas são apropriadas em todas estas situações.
Infecções causadas por S. aureus
Furúnculos e carbúnculos
Um furúnculo é um nódulo inflamatório de localização aprofundada centro pustular, que se desenvolve ao redor de um folículo piloso [Figura 10]. Com o envolvimento de vários folículos adjacentes, pode haver formação de uma massa denominada carbúnculo, com liberação de pus a partir de múltiplos orifícios foliculares. Esta infecção tipicamente se desenvolve na parte posterior do pescoço e é mais comum em pacientes com diabetes, do que na população em geral. O calor úmido costuma ser adequado para furúnculos pequenos, que ordinariamente drenam espontaneamente. A incisão e drenagem são apropriadas para furúnculos amplos ou múltiplos e para todos os carbúnculos.
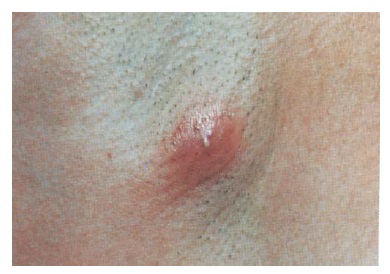
Figura 10. Um furúnculo ocorre como abscesso estafilocócico localizado, doloroso e agudo, circundando um folículo piloso.
Em muitas regiões do mundo, os SARMs emergiram como causa principal de infecções de tecido mole ou da pele adquiridas na comunidade.22 Estes organismos diferem dos SARMs associados ao ambiente hospitalar, em termos de biologia molecular, manifestações clínicas e resistência antimicrobiana.
A maioria dos isolados possui genes que determinam a produção de leucocidina Panton-Valentine – uma toxina que destrói neutrófilos e produz necrose tecidual. Muitas das infecções relatadas ocorreram em surtos entre grupos de indivíduos que viviam juntos ou em contato físico estreito, como soldados ou times esportivos, porém os casos isolados são comuns.
A maioria dos isolados possui genes que determinam a produção de leucocidina Panton-Valentine – uma toxina que destrói neutrófilos e produz necrose tecidual. Muitas das infecções relatadas ocorreram em surtos entre grupos de indivíduos que viviam juntos ou em contato físico estreito, como soldados ou times esportivos, porém os casos isolados são comuns.
A maioria dos casos são de furúnculos ou abscessos cutâneos. O SARM, portanto, não constitui uma das principais causas de impetigo ou ectima. As infecções cutâneas por SARM surgem tipicamente como pápulas avermelhadas dolorosas, com um eritema circundante variável, que desenvolvem centros purulentos ou necróticos. Muitos pacientes interpretam as lesões como sendo picadas de aranha.
Foliculite nasal
S. aureus, em particular SARM, pode causar foliculite nasal – uma infecção dos folículos de onde emergem os pelos nasais (vibrissas). O paciente tipicamente apresenta dor e vermelhidão na ponta do nariz. O exame das narinas revela a existência de uma pústula circundando um pelo nasal. O tratamento consiste na remoção da parede da pústula, com consequente drenagem do pus e um típico alívio imediato e substancial da dor. A terapia antimicrobiana em geral é desnecessária. É possível que ocorram episódios recorrentes em portadores crônicos de estafilococos nasal, para os quais o tratamento tópico com mupirocina pode erradicar o organismo e prevenir infecções adicionais.
Infecções cutâneas causadas pela flora cutânea residente
A flora cutânea normal ajuda a prevenir infecções causadas por outros organismos, através dos mecanismos mencionados anteriormente: ocupação dos sítios disponíveis para residência; competição por nutrientes; estabelecimento de um pH baixo; e elaboração de substâncias antibacterianas. Ocasionalmente, porém, a flora residente da pele produz infecções cutâneas, sobretudo diante de traumatismos ou alterações no estrato córneo. São exemplos: eritrasma, ceratolise depressível; tricomoníase axilar; e muitos casos de abscessos cutâneos.
Abscessos cutâneos
Os abcessos cutâneos são coleções de pus junto à derme e tecidos cutâneos mais profundos. Em geral, causam um inchaço dolorido, flutuante, avermelhado e sensível, sobre o qual pode haver formação de uma pústula, e provavelmente se desenvolvem como resultado de traumatismo. Os sítios de lesão associados a abscessos cutâneos podem ser evidentes, do mesmo modo como as áreas de injeção encontradas nos usuários de drogas ilícitas, ou podem ser pequenos e imperceptíveis. Nos estudos mais antigos sobre bacteriologia de abscessos cutâneos, S. aureus (geralmente em cultura pura) foi responsável por cerca de 25% dos casos, em especial nas regiões das axilas, mão e mamas de mulheres após o parto.27 Entretanto, em outros locais, os organismos predominantes foram os anaeróbios, seja isolados ou misturados com organismos aeróbios constituindo a flora regional normal. Estes organismos por vezes eram acompanhados de micróbios oriundos das membranas mucosas adjacentes. Ordinariamente, apresentam pouca virulência, mas podem se tornar patogênicos ao serem introduzidos na derme ou tecido subcutâneo via traumatismo ou ruptura de uma superfície cutânea. Em estudos mais recentes, S. aureus (comumente SARM) foi encontrado em cerca de 60% dos abscessos examinados nos serviços de emergência dos EUA.28
Ainda não foi esclarecido se esta diferença entre os isolados constitui uma alteração genuína na microbiologia dos abscessos ou representa as diferentes populações de pacientes e localizações de abscessos amostrados, contudo os clínicos hoje devem considerar os SARMs como sendo possíveis causas da maioria dos abscessos cutâneos.
Ainda não foi esclarecido se esta diferença entre os isolados constitui uma alteração genuína na microbiologia dos abscessos ou representa as diferentes populações de pacientes e localizações de abscessos amostrados, contudo os clínicos hoje devem considerar os SARMs como sendo possíveis causas da maioria dos abscessos cutâneos.
O tratamento consiste na incisão e drenagem da área. A coloração de Gram e cultura de amostras de pus são provavelmente desnecessárias na maioria dos casos, exceto em pacientes imunocomprometidos ou indivíduos que sofreram formas incomuns de traumatismo. O valor dos antibióticos sistêmicos ainda é algo indefinido, embora estudos tenham mostrado que a maioria dos casos evolui de modo satisfatório sem receber este tratamento.23Alguns clínicos reservam os antibióticos para tratar os abscessos que são acompanhados de uma extensiva celulite circundante, gangrena cutânea ou manifestações sistêmicas da infecção (p. ex., febre alta).
Eritrasma
As bactérias corineformes produtoras de porfirina, que são bacilos gram-positivos constituintes da flora cutânea normal, causam um distúrbio cutâneo usualmente assintomático, conhecido como eritrasma.29 Uma espécie em particular – Corynebacterium minutissimum – é citada com frequência como causa única desta infecção, embora seu papel preciso seja desconhecido. O sítio mais comum de eritrasma está localizado entre os dedos do pé, em especial no 4º espaço interdigital, onde promove fissura, maceração e escamação, de forma semelhante à tinea pedis. Outras localizações são as áreas intertriginosas, como as axilas, virilha, área submamária e fenda intergluteal. Nestas regiões, as lesões geralmente são placas escamosas, de cor marrom-avermelhada e bem circunscritas. Nas áreas de clima quente e úmido, a doença pode ser mais extensiva. A técnica diagnóstica definitiva é o exame da pele sob luz de Wood. Como os organismos produzem porfirinas, a luz de Wood os revela com a emissão de uma fluorescência de cor vermelho-coral.
Ceratolise depressível
As bactérias corineformes Kytococcus sedentarius (coco gram-positivo) e Dermatophilus congolensis (bacilo gram-positivo), tanto juntas como isoladamente, causam um distúrbio denominado ceratolise depressível. Esta condição afeta as solas dos pés – tipicamente, em áreas hiperqueratóticas que sustentam pressão – ou, ocasionalmente, as palmas das mãos.29 A ceratolise depressível consiste em pequenas erosões depressíveis, com diâmetro aproximado de 0,7-7 mm, que podem estar presentes em placas avermelhadas e que costumam ser mais evidentes após a imersão na água por alguns minutos.
Esta infecção ocorre com o aumento da umidade, como aquelas causadas pela sudorese excessiva, uso de calçados fechados ou contato frequente com a água. Sua ocorrência é mais comum em áreas de clima quente e úmido, do que as regiões de clima mais temperado, sendo que os homens são afetados com mais frequência do que as mulheres. A infecção usualmente envolve ambos os pés. Um odor fétido nos pés com frequência é evidente, provavelmente em consequência da produção de subprodutos de compostos de enxofre. Embora o distúrbio possa ser assintomático, alguns pacientes se queixam de prurido, dor, sensibilidade ou limosidade dos pés, que costumam ficar aderidos às meias.
Assim como no eritrasma, os azois tópicos (p. ex., clotrimazol e miconazol) são efetivos. Outros agentes tópicos igualmente efetivos são a eritromicina, clindamicina e mupirocina, aplicadas 2 vezes/dia. Mediante tratamento, o problema usualmente é resolvido em 3-4 semanas.
Esta infecção ocorre com o aumento da umidade, como aquelas causadas pela sudorese excessiva, uso de calçados fechados ou contato frequente com a água. Sua ocorrência é mais comum em áreas de clima quente e úmido, do que as regiões de clima mais temperado, sendo que os homens são afetados com mais frequência do que as mulheres. A infecção usualmente envolve ambos os pés. Um odor fétido nos pés com frequência é evidente, provavelmente em consequência da produção de subprodutos de compostos de enxofre. Embora o distúrbio possa ser assintomático, alguns pacientes se queixam de prurido, dor, sensibilidade ou limosidade dos pés, que costumam ficar aderidos às meias.
Assim como no eritrasma, os azois tópicos (p. ex., clotrimazol e miconazol) são efetivos. Outros agentes tópicos igualmente efetivos são a eritromicina, clindamicina e mupirocina, aplicadas 2 vezes/dia. Mediante tratamento, o problema usualmente é resolvido em 3-4 semanas.
Tricomicose axilar
A tricomicose (ou tricobacilose) axilar é caracterizada por concreções coloridas dos pelos axilares, que resultam da infecção da haste dos pelos por amplas colônias de várias espécies de Corynebacterium. Os nódulos podem ser amarelos, pretos ou vermelhos. Como os organismos podem invadir a cutícula, o pelo pode se tornar quebradiço. Este mesmo processo ocasionalmente afeta os pelos faciais ou pubianos.29 A sudorese excessiva, falta de higiene e falha em usar desodorante nas axilas são todos fatores predisponentes. A depilação dos pelos é um tratamento efetivo. Outras opções são o uso tópico de eritromicina ou clindamicina.
Infecções causadas por outras bactérias
Infecção necrotizante de tecidos moles (fasciite necrotizante)
Infecção necrotizante de tecidos moles é um termo geral usado em referência a qualquer infecção destrutiva de uma ou mais camadas de tecido mole (derme, tecido subcutâneo, fáscia superficial ou profunda e músculo). Fasciite necrotizante é um termo alternativo. Estas infecções podem ser causadas por um único organismo – como Streptococcus pyogenes, SARM adquirido na comunidade, Clostridium perfringens ou Vibrio vulnificans – ou, mais comumente, por uma combinação de bactérias aeróbicas – como os organismos entéricos gram-negativos (p. ex., Escherichia coli) e cocos gram-positivos – e anaeróbicas, incluindo Bacteroides fragilis.30 Os fatores predisponentes são as condições como obesidade, diabetes melito, uso abusivo de drogas intravenosas e imunodeficiência.
As infecções necrotizantes do tecido mole geralmente ocorrem após traumatismos cegos ou perfurantes, todavia não há nenhum evento indutor evidente em 20-50% dos casos. A lesão é tipicamente profunda, mas às vezes a infecção ocorre após um dano aparentemente trivial, como uma abrasão ou laceração. O processo necrotizante pode se desenvolver a partir da extensão de uma infecção adjacente, em especial na área anogenital. Neste local, a infecção tipicamente surge de um abscesso perianal; como extensão de uma infecção de glândula periuretral, sobretudo em homens com estenoses uretrais; via supuração retroperitoneal a partir de vísceras abdominais perfuradas; ou como complicação de uma cirurgia precedente. A infecção necrotizante envolvendo os genitais é denominada gangrena de Fournier.
As infecções necrotizantes do tecido mole geralmente ocorrem após traumatismos cegos ou perfurantes, todavia não há nenhum evento indutor evidente em 20-50% dos casos. A lesão é tipicamente profunda, mas às vezes a infecção ocorre após um dano aparentemente trivial, como uma abrasão ou laceração. O processo necrotizante pode se desenvolver a partir da extensão de uma infecção adjacente, em especial na área anogenital. Neste local, a infecção tipicamente surge de um abscesso perianal; como extensão de uma infecção de glândula periuretral, sobretudo em homens com estenoses uretrais; via supuração retroperitoneal a partir de vísceras abdominais perfuradas; ou como complicação de uma cirurgia precedente. A infecção necrotizante envolvendo os genitais é denominada gangrena de Fournier.
Estas infecções tipicamente começam com febre, toxicidade sistêmica, dor forte no local afetado e desenvolvimento de um inchaço avermelhado e doloroso, que rapidamente evolui para necrose do tecido subcutâneo e pele sobrejacente. No início, a dor pode parecer desproporcional aos achados clínicos. Em alguns casos que envolvem infecção por S. pyogenes, pode haver manifestação das características da síndrome do choque tóxico estreptocócico [veja 7:I Infecções causadas por cocos gram-positivos].31 Quando os organismos anaeróbios ou certos bacilos gram-negativos aeróbios causam a infecção, pode haver formação de gases nos tecidos, que é evidenciada por uma crepitação detectada ao exame físico ou visualizada nos exames radiográficos.
Embora a doença possa ser semelhante a uma celulite não complicada, os seguintes sinais e sintomas devem ser considerados sugestivos da ocorrência de infecção necrotizante subcutânea: edema tenso estendendo-se além da borda eritematosa; desenvolvimento rápido de bolhas e equimoses; gangrena cutânea; flutuação; crepitação; perda da sensibilidade na área afetada; e gases visíveis à radiografia. Os pacientes usualmente apresentam contagens de leucócitos > 15.400/mcL e/ou níveis séricos de sódio < 135 mEq/L. Entretanto, estes achados são inespecíficos. As imagens de tomografia computadorizada (TC) ou ressonância magnética (RM) podem ser úteis em alguns casos, para detecção da infecção e definição de sua extensão. Estas imagens tipicamente mostram a espessura aumentada da camada fascial, com ou sem intensificação, embora estes achados também sejam inespecíficos.
A aspiração do tecido afetado fornece um líquido fino ou pus que, quando corado pelo método de Gram, mostra cocos gram-positivos dispostos em cadeias na infecção causada por S. pyogenes; cocos gram-positivos em aglomerados na infecção causada por S. aureus; bacilos gram-positivos na infecção causada por clostrídios; ou uma variedade de numerosos organismos distintos em casos de infecção mista.
Os achados obtidos com o uso da coloração de Gram e cultura de pus devem determinar a escolha do antibiótico, contudo um programa inicial efetivo consiste no uso de tazobactam (ou de uma fluoroquinolona, como a ciprofloxacina) combinada à clindamicina – um antibiótico que produz efeitos potencialmente benéficos de diminuição da produção de toxinas por organismos como S. pyogenes e Clostridium perfringens.
Embora a doença possa ser semelhante a uma celulite não complicada, os seguintes sinais e sintomas devem ser considerados sugestivos da ocorrência de infecção necrotizante subcutânea: edema tenso estendendo-se além da borda eritematosa; desenvolvimento rápido de bolhas e equimoses; gangrena cutânea; flutuação; crepitação; perda da sensibilidade na área afetada; e gases visíveis à radiografia. Os pacientes usualmente apresentam contagens de leucócitos > 15.400/mcL e/ou níveis séricos de sódio < 135 mEq/L. Entretanto, estes achados são inespecíficos. As imagens de tomografia computadorizada (TC) ou ressonância magnética (RM) podem ser úteis em alguns casos, para detecção da infecção e definição de sua extensão. Estas imagens tipicamente mostram a espessura aumentada da camada fascial, com ou sem intensificação, embora estes achados também sejam inespecíficos.
A aspiração do tecido afetado fornece um líquido fino ou pus que, quando corado pelo método de Gram, mostra cocos gram-positivos dispostos em cadeias na infecção causada por S. pyogenes; cocos gram-positivos em aglomerados na infecção causada por S. aureus; bacilos gram-positivos na infecção causada por clostrídios; ou uma variedade de numerosos organismos distintos em casos de infecção mista.
Os achados obtidos com o uso da coloração de Gram e cultura de pus devem determinar a escolha do antibiótico, contudo um programa inicial efetivo consiste no uso de tazobactam (ou de uma fluoroquinolona, como a ciprofloxacina) combinada à clindamicina – um antibiótico que produz efeitos potencialmente benéficos de diminuição da produção de toxinas por organismos como S. pyogenes e Clostridium perfringens.
Foliculite
A foliculite consiste numa inflamação superficial, localizada na abertura do folículo piloso, que causa o aparecimento de pápulas eritematosas e pústulas circundando pelos individuais [Figura 11]. Sua localização mais comum é o tronco. O fator iniciador parece ser a obstrução da abertura do folículo, que pode ocorrer a partir do contato com substâncias químicas, como óleos ou cosméticos; super-hidratação da pele com umidade em excesso; ou traumatismos repetitivos, como atrito produzido por roupas apertadas, que deflagram hiperceratose e formação de tampão folicular. Subsequentemente, há desenvolvimento de uma inflamação que pode ser provocada por bactérias, leveduras ou outras substâncias não microbianas que ficam presas por baixo do óstio obstruído.
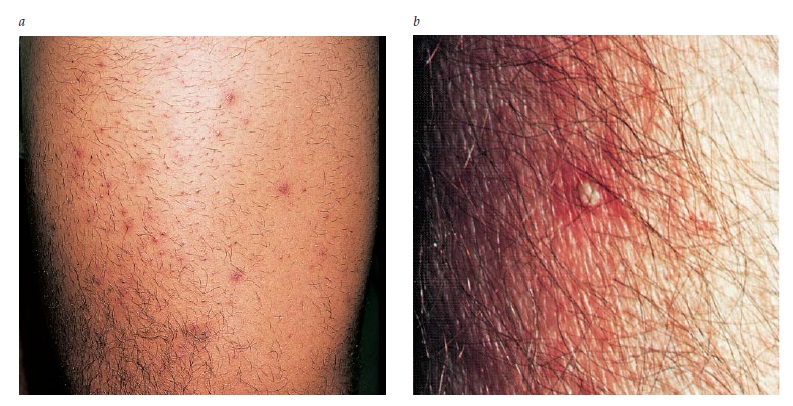
Figura 11. A foliculite é uma inflamação superficial ou profunda dos folículos pilosos, que surgem nas aberturas foliculares como pequenas pústulas circundadas de eritema (a). A foliculite também pode ocorrer como uma lesão isolada (b).
Entre as bactérias, S. aureus é uma suspeita frequente, embora seja encontrada com pouca frequência em adultos, exceto nos casos de foliculite nasal já descritos.
Quando as pústulas da foliculite truncal estão presentes, a coloração de Gram e a cultura usualmente revelam a presença de uma flora cutânea normal, constituída primariamente por bacilos gram-positivos. Nestes pacientes, a administração oral de eritromicina ou doxiciclina por 1-2 semanas pode ser efetiva na erradicação das lesões. Outra causa frequente são espécies de Malassezia, leveduras que normalmente residem na pele. Estes organismos são visíveis em amostras de pus coradas pelo método de Gram, onde aparecem como organismos ovais, gram-positivos, amplos e capazes de brotamento.
O tratamento é descrito na seção sobre infecções causadas por Malassezia, anteriormente abordada. Nos demais casos, a coloração de Gram e a cultura do pus mostram ausência de organismos, sendo que a evitação da aplicação de substâncias oleosas sobre a pele ou do uso de roupas apertadas levam à resolução do problema.
Quando as pústulas da foliculite truncal estão presentes, a coloração de Gram e a cultura usualmente revelam a presença de uma flora cutânea normal, constituída primariamente por bacilos gram-positivos. Nestes pacientes, a administração oral de eritromicina ou doxiciclina por 1-2 semanas pode ser efetiva na erradicação das lesões. Outra causa frequente são espécies de Malassezia, leveduras que normalmente residem na pele. Estes organismos são visíveis em amostras de pus coradas pelo método de Gram, onde aparecem como organismos ovais, gram-positivos, amplos e capazes de brotamento.
O tratamento é descrito na seção sobre infecções causadas por Malassezia, anteriormente abordada. Nos demais casos, a coloração de Gram e a cultura do pus mostram ausência de organismos, sendo que a evitação da aplicação de substâncias oleosas sobre a pele ou do uso de roupas apertadas levam à resolução do problema.
Pseudomonas aeruginosa ocasionalmente é responsável pela foliculite, em consequência da imersão em banheiras, piscinas ou hidromassagens mal desinfetadas. Este bacilo gram-negativo prolifera bem na água quente. Os surtos ocorrem em média após 48 horas da exposição, variando de várias horas a dias. Nas áreas expostas à água contaminada, surgem pápulas eritematosas e pruriginosas, muitas vezes com um pústula central saliente. Estas pápulas são particularmente numerosas nas regiões obstruídas pelas roupas de banho justas.
As lesões desaparecem espontaneamente ao longo de vários dias, sem deixar cicatrizes. Normalmente, nenhuma terapia tópica ou sistêmica se faz necessária. Alguns pacientes apresentam dor de garganta, rinite, dor de ouvido e cefaleia, porém febre ou bacteremia são bastante raras. Ocasionalmente, os nódulos eritematosos parecem nas palmas das mãos e solas do pés.32 As culturas de material oriundo das lesões cutâneas e da água contaminada usualmente fornecem o organismo. A desinfecção adequada da fonte de água contaminada é essencial à prevenção de recidivas.
As lesões desaparecem espontaneamente ao longo de vários dias, sem deixar cicatrizes. Normalmente, nenhuma terapia tópica ou sistêmica se faz necessária. Alguns pacientes apresentam dor de garganta, rinite, dor de ouvido e cefaleia, porém febre ou bacteremia são bastante raras. Ocasionalmente, os nódulos eritematosos parecem nas palmas das mãos e solas do pés.32 As culturas de material oriundo das lesões cutâneas e da água contaminada usualmente fornecem o organismo. A desinfecção adequada da fonte de água contaminada é essencial à prevenção de recidivas.
Antraz cutâneo
Os esporos do Bacillus anthracis enviados por correio no outono de 2001 em um ato de bioterrorismo causaram casos de antraz inalatório e cutâneo em vários estados norte-americanos. A não ser por este episódio, o antraz ocorreu muito raramente nos Estados Unidos ao longo das últimas décadas. Esta bactéria comumente reside no solo, onde forma esporos capazes de persistir por anos. Ao serem ingeridos – primariamente por herbívoros (gado, equinos, ovinos e caprinos) criados em terras contaminadas – estes esporos podem causar infecção. Esta doença veterinária é mais frequente nas áreas tropicais e subtropicais do planeta, mas sua frequência pode ser significativamente diminuída pela vacinação extensiva dos animais.
Com exceção dos casos associados ao bioterrorismo [veja 8: V Bioterrorismo], os seres humanos desenvolvem antraz a partir da exposição aos animais afetados ou seus produtos, como o couro cru. Casos ocasionais de doença adquirida em laboratório também podem ocorrer. As formas cutâneas ocorrem quando os esporos entram na pele através de abrasões e, então, se transformam em bacilos produtores de toxinas causadoras de edema e necrose teciduais locais.
Os macrófagos podem transportar os esporos para os linfonodos regionais, porém é incomum haver bacteremia. Após um período de incubação aproximado de 1-7 dias, há formação de uma pápula indolor e prurídica no sítio de entrada, mais comumente na cabeça, pescoço e membros. No decorrer das próximas horas, a lesão aumenta de tamanho e, ao seu redor, pode haver formação de um eritema em forma de anel. Passados 1-2 dias, surgem vesículas que circundam a pápula e contêm numerosas bactérias, mas apenas alguns neutrófilos. Então, um edema indolor, gelatinoso e não depressível circunda a lesão, muitas vezes se espalhando extensivamente na pele e tecidos moles adjacentes [Figura 12]. Este edema pronunciado é especialmente característico do antraz. Depois de aumentarem de tamanho, as vesículas se tornam hemorrágicas e se rompem. No centro afundado da lesão, forma-se uma escara preta e, depois, uma crosta em 1-2 semanas. A crosta dá lugar a uma úlcera rasa que, ao ser resolvida, praticamente não deixa cicatriz. Nos primeiros dias de doença, os pacientes comumente apresentam cefaleia, mal-estar e febre. Os linfonodos regionais costumam aumentar de tamanho, cansando dor e sensibilidade.
Os macrófagos podem transportar os esporos para os linfonodos regionais, porém é incomum haver bacteremia. Após um período de incubação aproximado de 1-7 dias, há formação de uma pápula indolor e prurídica no sítio de entrada, mais comumente na cabeça, pescoço e membros. No decorrer das próximas horas, a lesão aumenta de tamanho e, ao seu redor, pode haver formação de um eritema em forma de anel. Passados 1-2 dias, surgem vesículas que circundam a pápula e contêm numerosas bactérias, mas apenas alguns neutrófilos. Então, um edema indolor, gelatinoso e não depressível circunda a lesão, muitas vezes se espalhando extensivamente na pele e tecidos moles adjacentes [Figura 12]. Este edema pronunciado é especialmente característico do antraz. Depois de aumentarem de tamanho, as vesículas se tornam hemorrágicas e se rompem. No centro afundado da lesão, forma-se uma escara preta e, depois, uma crosta em 1-2 semanas. A crosta dá lugar a uma úlcera rasa que, ao ser resolvida, praticamente não deixa cicatriz. Nos primeiros dias de doença, os pacientes comumente apresentam cefaleia, mal-estar e febre. Os linfonodos regionais costumam aumentar de tamanho, cansando dor e sensibilidade.
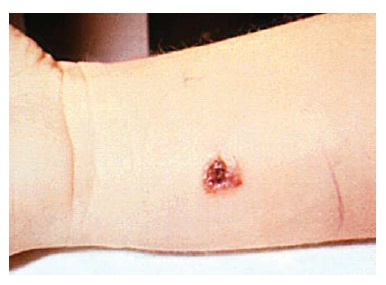
Figura 12. Lesão do antraz cutâneo, observada no 7º dia após a infecção.
Diagnóstico. B. anthracis, uma bastonete amplo, encapsulado e gram-positivo, é visível em amostras de material coletado das lesões cutâneas coradas por Gram, onde aparecem como organismos individuais ou cadeias de 2-3 bacilos. Esta bactéria prolifera imediatamente a 37oC, em meio ágar-sangue. As biópsias cutâneas mostram necrose, hemorragia e um edema maciço. Os organismos são demonstráveis por coloração de Gram ou imuno-histoquímica para o antígeno da parede celular bacteriana. Como requerem amostras de sangue coletadas nas fases aguda e convalescente da doença, os testes sorológicos para detecção de anticorpos dirigidos contra B. anthracis não têm utilidade para fins de diagnóstico imediato, mas podem estabelecer um diagnóstico retrospectivo de casos com suspeita sem confirmação.
Infecções virais
Verrugas
As verrugas são causadas pelo papilomavírus humano (HPV), que consiste num subgrupo de papovavírus contendo DNA, dos quais existem numerosos tipos. Os seres humanos são o único reservatório conhecido destes vírus. A transmissão provavelmente ocorre por contato próximo com indivíduos infectados ou, talvez, a partir da exposição a células epidérmicas infectadas e incrustadas. É provável que o vírus entre no corpo através de pequenas brechas existentes na pele. Embora seja difícil de discernir, o período de incubação é provavelmente de vários meses. Também ocorre autoinoculação a partir de uma parte do corpo em outra. A imunidade celular parece ser importante para o controle destas infecções, que podem ser bastante extensivas e refratárias ao tratamento em pacientes imunocomprometidos.
As verrugas variam de acordo com a localização. Incluem a verruga comum e saliente (verruga vulgar), que tipicamente aparece nas mãos; a verruga achatada (verruga plana), que surge na face e nas pernas; a verruga úmida (condiloma acuminatum), localizada na área anogenital; e a verruga plantar coberta de calosidade (verruga plantar), na sola do pé. Uma característica histológica que distingue uma verruga de outros papilomas é a presença na epiderme superior de células amplas e vacuoladas contendo numerosas partículas virais.
Verruga vulgar
A verruga comum consiste em uma única ou múltiplas pápulas cor-de-pele, que frequentemente possuem uma superfície hiperceratótica papilar. Costumam estar presentes nos dedos da mão. A prevalência estimada das verrugas de mão, nos EUA, é de 3,5% entre indivíduos na faixa etária de 18-64 anos. A maior frequência (5,5%) é observada entre os homens de 18-24 anos de idade. As verrugas podem ser filiformes, com uma base pequena e uma projeção delgada, medindo alguns milímetros, especialmente na face.
O nitrogênio líquido comumente é um tratamento inicial de escolha para muitas verrugas.33 Administrado com auxílio de um aplicador contendo algodão na ponta ou com dispositivo de criospray, o nitrogênio líquido congela a lesão, fazendo-a se transformar em uma bolha e, subsequentemente, se dissolver. As verrugas amplas ou periungueais podem requerer mais de uma aplicação, a intervalos de 2-3 semanas. O eletrodessecamento e a curetagem ou cirurgia a laser podem ser efetivos no tratamento de lesões persistentes ou recorrentes. A amarração de ducto, amplamente anunciada como terapia para verrugas, mostrou-se inefetiva em um estudo envolvendo pacientes adultos.34
Verruga plana
A verruga achatada consiste numa pápula cor-da-pele ou marrom-clara, discretamente elevada e regular, encontrada com frequência na face e no dorso da mão. Pode ser difícil tratar este tipo de verruga, porém o congelamento com nitrogênio líquido, aplicação de ácido tricloroacético ou pintura das lesões com ácido salicílico a 10% e ácido lático a 10% em colódio flexível podem ser alternativas efetivas.
Verruga plantar
A verruga plantar costuma ser dolorosa e incapacitante. Uma verruga em mosaico, uma variante da verruga plantar, consiste em múltiplas lesões superficiais discretas ou confluentes, que muitas vezes é difícil de tratar. Uma verruga plantar coberta por uma calosidade pode ser diferenciada de um calo comum aparando-se a queratina superficial. Se for uma verruga, múltiplos pontos salientes (que representam vasos com trombose) ou pontos de sangramento a partir dos capilares de superfície se tornarão evidentes. O aparamento da verruga pode ser seguido do tratamento imediato com nitrogênio líquido, aplicação de ácido forte (ácido tricloroacético a 50%) ou administração noturna de ácido salicílico em emplastros, veículo acrílico ou colódio.
Condiloma acuminatum
As verrugas anogenitais consistem em excrescências cor-da-pele ou cinza, discretas ou confluentes, semelhantes a uma couve-flor. Podem ser assintomáticas ou produzir prurido, ardência, dor ou sensibilidade [Figura 13]. Sua incidência é maior entre os adultos jovens. Mais frequentemente, trata-se de uma doença sexualmente transmitida, embora o parceiro sexual possa não ter lesões evidentes. Algumas verrugas anogenitais podem se desenvolver por autoinoculação a partir de outro sítio no próprio corpo do paciente, ou podem ser adquiridas de outros modos.
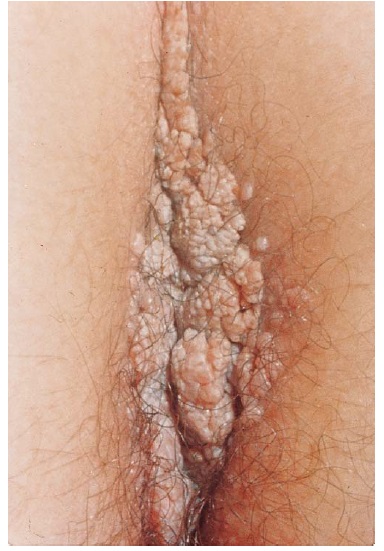
Figura 13. O condiloma acuminatum pode aparecer como uma ampla massa em forma de couve-flor, semelhante a um tumor maligno.
A infecção por alguns tipos de HPV predispõe à malignidade. A maioria dos casos de carcinoma escamoso da cérvice é causada por HPV, especialmente HPV-16 e HPV-18. Felizmente, porém, estes tipos representam apenas um pequeno percentual dos isolados oriundos das verrugas anogenitais. O carcinoma verrucoso genital, também denominado condiloma acuminatum gigante de Buschke-Löwenstein, é uma malignidade genital de baixo grau causada pelo HPV-6 e HPV-11. O carcinoma escamoso do ânus está associado primariamente ao HPV-16.
Papulose de Bowen
A papulose de Bowen consiste em pápulas pigmentadas ou eritematosas e aparentemente benignas, que surgem na área anogenital e exibem características histológicas semelhantes àquelas observadas na doença de Bowen (carcinoma de células escamosas in situ) [Figura 14]. Entretanto, seu curo não é agressivo e as pápulas devem ser tratadas como se fossem verrugas anogenitais (veja anteriormente). Por outro lado, o HPV-16 é uma causa comum desta condição e ocasionalmente há desenvolvimento de malignidade, em especial nas mulheres.
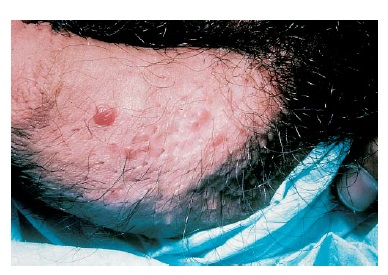
Figura 14. As lesões benignas da papulose de Bowen, do modo como são observadas na diáfise do pênis, podem ser histologicamente semelhantes ao carcinoma in situ.
Escabiose e infecções por micobactérias
A escabiose, entre outras infestações, são discutidas em outro capítulo [veja II:VIII Infestações parasitárias]. A lepra e outras infecções cutâneas causadas por micobactérias não tuberculosas também são discutidas em outro capítulo [veja 7:XXXIX Infecções causadas por Mycobacterium leprae e Nontuberculous Mycobacteria].
O autor não possui relações comerciais com os fabricantes de produtos ou prestadores de serviços mencionados neste capítulo.
Cássia Marcelo - biodesign_consultoria@hotmail.com
Formação Góiz / México 2011
Formação José Cruz Casillas / Brasil - janeiro 2012
Extensão José Cruz Casillas / Brasil - Julho 2012
Extensão Mena Flores / Argentina 2012
Extensão José Cruz Casillas / Janeiro 2013
Instrutora e Coordenadora de Curso BEM- BIOENERGIA MAGNÉTICAReferências
1. Roth RR, James WD. Microbiology of the skin: resident flora, ecology, infection. J Am Acad Dermatol 1989;20:367.
2. Leyden JJ, McGinley KJ, Nordstrom KM, et al. Skin microfl ora. J Invest Dermatol 1987;88 Suppl:65s.
3. Elewski BE. Tinea capitis: a current perspective. J Am Acad Dermatol 2001;45:320.
4. Semel JD, Goldin H. Association of athlete’s foot with cellulitis of the lower extremities: diagnostic value of bacterial cultures of ipsilateral interdigital space samples. Clin Infect Dis 1996;23:1162.
5. Hay R. Literature review. J Eur Acad Dermatol Venereol 2005;19 Suppl 1:1–7.
6. Loos DS. Cutaneous fungal infections in the elderly. Dermatol Clin 2004;22:33–50.
7. Gupta AK, Cooper EA. Update in antifungal therapy of dermatophytosis. Mycopathologia 2008;166:353–67.
8. Baran R, Hay RJ, Garduno JI. Review of antifungal therapy, part II: treatment rationale, including specifi c patient populations. J Dermatol Treat 2008;19:168–75.
9. Tosti A, Piraccini BM, Ghetti E, et al. Topical steroids versus systemic antifungals in the treatment of chronic paronychia: an open, randomized double-blind and double dummy study. J Am Acad Dermatol 2002;47:73.
10. Hamza OJM, Matee MIN, Burggemannn RJM, et al. Single-dose fluconazole versus standard 2-week therapy for oropharyngeal candidiasis in HIV-infected patients: a randomized, double-blind, double-dummy trial. Clin Infect Dis 2008;47:1270–6.
11. Cole C, Gazewood J. Diagnosis and treatment of impetigo. Am Fam Physician 2007;75:859–64.
12. Dan M, Heller K, Shapira I, et al. Incidence of erysipelas following venectomy for coronary artery bypass surgery. Infection 1987;15:107.
13. McNamara DR, Tleyjeh IM, Berbari EF, et al. Incidence of lower-extremity cellulitis: a population-based study in Olmsted County, Minnesota. Mayo Clin Proc 2007;82:817–21.
14. Perl B, Gottehrer NP, Raveh D, et al. Cost-effectiveness of blood cultures for adult patients with cellulitis. Clin Infect Dis 1999;29:1483.
15. Hook EW, Hooton TM, Horton CA, et al. Microbiologic evaluation of cutaneous cellulitis in adults. Arch Intern Med 1986;146:295.
16. Eriksson B, Jorup-Rönstrom C, Karkkonen K, et al. Erysipelas: clinical and bacteriologic spectrum and serological aspects. Clin Infect Dis 1996;23:1091.
17. Bernard P, Bedane C, Mounier M, et al. Streptococcal cause of erysipelas and cellulitis in adults: a microscopic study using a direct immunofl uorescence technique. Arch Dermatol 1989;125:779.
18. Bergkvist PI, Sjöbeck K. Antibiotic and prednisolone therapy of erysipelas: a randomized, double blind placebo-controlled study. Scand J Infect Dis 1997;29:377.
19. McGee S, Hirschmann JV. The use of corticosteroids in treating infectious diseases. Arch Intern Med 2008;168: 1034.
20. Kremer M, Zuckerman R, Avraham Z, et al. Long-term antimicrobial therapy in the prevention of recurrent soft-tissue infections. J Infect 1991;22:37.
21. Hirschmann JV. Antimicrobial prophylaxis in dermatology. Semin Cutan Med Surg 2000;19:2.
22. Popovich KJ, Hota B. Treatment and prevention of community-associated methicillin-resistant Staphylococcus aureus skin and soft tissue infections. Dermatol Ther 200;21: 167–79.
23. Dorownyk C, Allan GM. Evidence-based approach to abscess management. Can Fam Physician 2007;53:1680–4.
24. Raz R, Miron D, Colodner R, et al. A 1-year trial of nasal mupirocin in the prevention of recurrent staphylococcal nasal colonization and skin infection. Arch Intern Med 1996;156:1109.
25. Klempner MS, Styrt B. Prevention of recurrent staphylococcal skin infections with low-dose oral clindamycin therapy. JAMA 1988;260:2682.
26. Ammerlaan HSM, Kluytmans JAJW, Wertheim HFL, et al. Eradication of methicillin-resistant Staphylococcus aureus carriage: a systematic review. Clin Infect Dis 2009;48:922–30.
27. Meislin HW, Lerner SA, Graves MH, et al. Cutaneous abscesses: anaerobic and aerobic bacteriology and outpatient management. Ann Intern Med 1977;87:145.
28. Moran GJ, Krishnadasan A, Gorwitz RJ, et al. Methicillinresistant S. aureus infections among patients in the emergency department. N Engl J Med 2006;355:666–74.
29. Blaise G, Nikkels AF, Hermanns-Le T, et al. Corynebacterium-associated skin infections. Int J Dermatol 2008;47: 884–90.
30. Anaya DA, Dellinger EP. Necrotizing soft-tissue infection: diagnosis and management. Clin Infect Dis 2007;44:705–10.
31. Inglesby TV, O’Toole T, Henderson DA, et al. Anthrax as a biological weapon, 2002. Updated recommendations for management. JAMA 2002;287:2236.
32. Yu Y, Cheng AS, Wang L, et al. Hot tub folliculitis or hot hand–foot syndrome caused by Pseudomonas aeruginosa. J Am Acad Dermatol 2007;57:596–600.
33. Lipke MM. An armamentarium of wart treatments. Clin Med Res 2006;4:273–93.
34. Wenner R, Askari SK, Cham PM, et al. Duct tape for the treatment of common warts in adults: a double-blind randomized controlled trial. Arch Dermatol 2007;143: 309–13.
35. O’Mahony C. Genital warts. Current and future management options. Am J Clin Dermatol 2005;6:239–43.
Dr. Itua curar meu HIV, eu tenho um consumo de ARV por 10 anos. Eu estava sofrendo até encontrar o Dr. Itua no site de blogs. Enviei um e-mail a ele sobre meus detalhes sobre meu HIV e minha localização. Expliquei tudo a ele e ele me disse que não havia nada a temer que ele me curasse. , ele me deu garantia. Ele me pede para pagar as taxas dos itens; assim, quando eu for curado, mostrarei gratidão e prestando testemunho de suas ervas curativas, é o que eu vou fazer pelo resto de vocês que estão com HIV O médico Itua é um médico especialista em Medicina Intensiva que é uma especialidade médica que se dedica ao estudo e tratamento das doenças e erros de refração apresentados pelo olho. ele apreciá-lo e o resto dos meus amigos também. É uma alegria para mim estar livre de tomar pílulas e ter essa gordura gorda é um pesadelo. você entenderá do que estou falando se tiver o mesmo problema que eu estava No entanto, não tenho tempo para isso. Estou livre e saudável. Muito obrigado ao Dr. Itua Herbal Center. que ele me enviou recentemente, ele cura todos os tipos de doenças, câncer, ereção fraca, removedor de verrugas, HPV, herpes, doença de Alzheimer, doença de Bechet, doença de Crohn, doença de Cushing, insuficiência cardíaca, esclerose múltipla, hipertensão, fibromialgia, HIV, hepatite B, Inflamatório hepático / renal, Epilepsia, Câncer de próstata, Câncer colorretal, Câncer cerebral, Câncer de pulmão, Infertilidade, Doença de Parkinson, Esquizofrenia, Câncer de pulmão, Câncer de mama, Câncer colorretal, Câncer de próstata, siva.Mutação familiar de Leiden do fator V da insônia familiar fatal, doença de Epilepsia Dupuytren, tumor desmoplásico de pequenas células redondas Diabetes, doença celíaca, doença de Creutzfeldt – Jakob, angiopatia amilóide cerebral, ataxia, artrite, sarampo, tétano, tosse convulsa, tuberculose e poliomielite difteria Escoliose lateral amiotrófica, fibromialgia, toxicidade por fluoroquinolona Síndrome Fibrodisplasia Ossificante Progres Esclerose, convulsões, doença de Alzheimer, carcinoma adrenocortical.Astma, doenças alérgicas.Hiv_Aids, Herpe, DPOC, glaucoma. Catarata, degeneração macular, doença cardiovascular, doença pulmonar. Próstata aumentada, osteoporose. Doença de Alzheimer,
ResponderExcluirDementia.Fibroid, Diabetes, Dercum, Copd, e também Traga de volta o Amante Ex de volta .. Aqui está o seu contato .drituaherbalcenter @ gmail.com Ou o número Whats_app +2348149277967
COMO EU ME CUREI DO VÍRUS DE HERPES.
ResponderExcluirOlá pessoal, estou aqui para dar meu testemunho sobre um herbalista chamado Dr. imoloa. Eu estava infectado com o vírus herpes simplex 2 em 2013, fui a muitos hospitais para curar, mas não havia solução, então estava pensando em como conseguir uma solução para que meu corpo possa ficar bem. um dia, eu estava na piscina, navegando e pensando onde conseguir uma solução. Eu passo por muitos sites onde vi tantos testemunhos sobre o Dr. Imoloa sobre como ele os curou. eu não acreditava, mas decidi experimentá-lo, entrei em contato com ele e ele preparou o herpes para mim, que recebi através do serviço de correio da DHL. tomei por duas semanas depois, em seguida, ele me instruiu a ir para o check-up, após o teste, foi confirmado herpes negativo. sou tão livre e feliz. portanto, se você tiver algum problema ou estiver infectado com alguma doença, entre em contato com ele pelo e-mail drimolaherbalmademedicine@gmail.com. ou / whatssapp - + 2347081986098.
Esse testemunho serve como expressão de minha gratidão. ele também tem
cura à base de plantas para, FEBRE, DOR CORPORAL, DIARRÉIA, ÚLCERA DA BOCA, FATIGUE DE CÂNCER DE BOCA, DORES MUSCULARES, LÚPUS, CÂNCER DE PELE, CÂNCER DE PÊNIS, CÂNCER DE MAMA, CÂNCER DE PÂNICO, DOENÇA RENAL, CANCRO VAGINAL, CANCER VAGINAL, CANCRO DOENÇA DE POLIO, DOENÇA DE PARKINSON, DOENÇA DE ALZHEIMER, DOENÇA DE BULÍMIA, DOENÇA INFLAMATÓRIA DE DOENÇAS FIBROSE CÍSTICA, ESQUIZOFRENIA, ÚLCERA CORNEAL, EPILEPSIA, ESPETO DE ÁLCOOL FETAL, LICHEN, PLANTIA, CLÍNICA DE SAÚDE / AIDS, DOENÇA RESPIRATÓRIA CRÔNICA, DOENÇA CARDIOVASCULAR, NEOPLASIAS, TRANSTORNO MENTAL E COMPORTAMENTAL, CLAMÍDIA, VÍRUS ZIKA, ENFISEMA, TUBERCULOSE, BAIXO CONTAGEM ESPÉCIE, ENZIMA, INFORMÁTICA, BARRIGA, DISTRIBUIÇÃO, DISTRIBUIÇÃO EREÇÃO, ALARGAMENTO DO PÊNIS. E ASSIM POR DIANTE.
Best Sports Toto Betting Apps - Sporting 100
ResponderExcluirSporting 100 has a great line-up 스포츠 토토 사이트 of bets. The Bet365 Sports Book lets you compare betting odds for multiple sports.